La nostra équipe

Dedichiamo ad ogni coppia
tutte le nostre attenzioni.
Ogni coppia ha la sua storia fatta di aspettative, tentativi ed emozioni. Il nostro principale impegno è ascoltarle e comprenderle da vicino, prima di tutto sotto il profilo umano ed emotivo e subito dopo sotto quello scientifico e terapeutico.
Condividere il percorso personale fatto prima di arrivare alla decisione di intraprendere l’iter di Procreazione Assistita è per noi un aspetto fondamentale, perché rappresenta il primo passo per instaurare con ciascuna coppia una relazione di stima e fiducia indispensabile per compiere insieme il viaggio verso una nuova vita con serenità e ottimismo.

Dedichiamo ad ogni coppia
tutte le nostre attenzioni.
Ogni coppia ha la sua storia fatta di aspettative, tentativi ed emozioni. Il nostro principale impegno è ascoltarle e comprenderle da vicino, prima di tutto sotto il profilo umano ed emotivo e subito dopo sotto quello scientifico e terapeutico.
Condividere il percorso personale fatto prima di arrivare alla decisione di intraprendere l’iter di Procreazione Assistita è per noi un aspetto fondamentale, perché rappresenta il primo passo per instaurare con ciascuna coppia una relazione di stima e fiducia indispensabile per compiere insieme il viaggio verso una nuova vita con serenità e ottimismo.
Come si svolge il percorso di coppia?
Prenotazione e Accettazione
Per accedere al Centro di Procreazione di Villa Margherita non dovrai fare file d’attesa, ma solo prendere appuntamento!
La nostra responsabile avrà cura di fissarlo il prima possibile, venendo incontro alle tue esigenze di coppia e indicandoti la procedura
da seguire e i documenti da portare con te.
Primo Appuntamento
La nostra responsabile all’accettazione ti accoglierà in un ambiente discreto e familiare, procedendo alla registrazione dei tuoi dati e assegnandoti un codice di coppia personale.
La nostra Equipe sarà a tua completa disposizione
per fornirti la migliore assistenza.
Prima Visita di Coppia
Durante la prima visita verrà inquadrata la tua situazione di coppia dal punto di vista clinico e verranno effettuati i primi
accertamenti (ecografia pelvica, conta riserva ovarica, spermiogramma). In tale
occasione riceverai la lista completa di tutti gli esami propedeutici al trattamento.
Definizione Percorso PMA
Una volta effettuati gli esami prescritti e accertamenti, verrà stabilito il tuo piano terapeutico di coppia. Il Responsabile del Trattamento spiegherà le procedure di PMA scelte in base al quadro clinico emerso, illustrando l’iter e la metodica più idonea a raggiungire
il risultato sperato.
Stimolazione Ovarica e Monitoraggio
I trattamenti di PMA iniziano con la fase di
stimolazione della multiovulazione che viene eseguita in modo mirato e personalizzato. Durante questo step monitoreremo la tua crescita follicolare per capire il momento migliore per effettuare l’inseminazione intrauterina o il prelievo ovocitario.
PMA di 1° Livello (IUI)
L’inseminazione intrauterina è una tecnica di riproduzione assistita “in vivo” che consente di facilitare l’incontro tra lo spermatozoo e l’ovocita. Tale trattamento prevede una moderata stimolazione farmacologica. Viene spesso consigliata nei casi di sterilità inspiegata e quando la funzionalità tubarica non presenta alcun problema.
PMA di 2° Livello (FIVET/ICSI)
Il trattamento PMA di secondo livello consiste in specifiche tecniche di fecondazione “in vitro” che prevedono il prelievo dei gameti (Pick-up ovocitario), la raccolta e il trattamento del liquido seminale, l’inseminazione e coltura embrionaria seguita dal transfer degli embrioni e/o la loro crioconservazione.
LA PMA DI TIPO ETEROLOGO
La fecondazione eterologa è una tecnica di PMA che si esegue attraverso la donazione di gameti femminili (ovociti) o maschili (spermatozoi). La donazione dev’essere volontaria, cioè frutto di una scelta intenzionale e consapevole, e disinteressata, ossia non può essere effettuata dietro compenso.
Approfondisci…
Le tecniche più avanzate di procreazione assistita.
La IUI è una tecnica che consiste nel rilascio nell’utero di un’aliquota di liquido seminale mediante un sottile catetere.
La IUI, inseminazione intrauterina, che consiste nell’inserire, mediante un sottile catetere in utero, il liquido seminale opportunamente preparato, rappresenta il primo livello della fecondazione assistita.
La IUI viene consigliata ed eseguita quando si suppone che, nella coppia, vi sia solo un impedimento per il raggiungimento degli ovociti da parte degli spermatozoi e può essere eseguita durante un ciclo spontaneo o in seguito ad una lieve stimolazione farmacologica.
Le indicazioni secondo le linee guida della legge 40/2004 sono:
-
sterilità inspiegata
-
infertilità maschile di grado lieve-moderato
-
endometriosi I-II stadio e casi selezionati di III-IV stadio della classificazione American Fertility Society (AFS) in particolare dopo l’intervento chirurgico
-
ripetuti insuccessi di induzione della gravidanza con stimolazione dell’ovulazione e rapporti mirati
-
patologie sessuali e coitali che non hanno trovato giovamento dall’inseminazione intracervicale semplice
-
fattore cervicale
La IUI ha come percentuale si successo un valore che varia dal 5 al 12%, a seconda dell’età della donna e di altri fattori. Si deve considerare che, nei rapporti spontanei di una coppia fertile, la possibilità di concepire naturalmente è del 20-25% fino ai 35 anni e del 15- 20% dai 35 ai 40.
Quando la IUI è la prima strada da percorrere, si consiglia di effettuare almeno tre tentativi, prima di procedere con altri trattamenti, quali la FIVET o l’Iniezione intracitoplasmatica degli spermatozoi (ICSI).
Nella FIVET gli ovociti prelevati vengono posti a contatto diretto con gli spermatozoi.
Nella FIVET, acronimo di In Vitro Fertilization and Embryo Transfer, gli ovociti ancora circondati dalle cellule del cumulo ooforo vengono posti a diretto contatto con gli spermatozoi.
Così facendo, mediante una selezione naturale, solo lo spermatozoo riesce a penetrare all’interno dell’ovocita ed a dar vita al processo della fecondazione.
Secondo alcuni, è una metodica più naturale e fisiologica della ICSI, in quanto la selezione dello spermatozoi non avviene ad opera dell’embriologo.
Per poter effettuare una fecondazione in vitro è necessario che le caratteristiche iniziali del liquido seminale siano tali da poter ottenere una concentrazione di spermatozoi mobili adeguata (almeno 100.000 spermatozoi mobili per ovocita).
La FIVET, nei casi di alterata morfologia degli spermatozoi (teratospermia) non è consigliata in quanto la struttura alterata, soprattutto quella della testa (regione acrosomiale) potrebbe ridurre la capacità della spermatozoo di interagire con l’involucro esterno dell’ovocita e quindi impedire la fertilizzazione.
Le indicazioni secondo le linee guida della legge 40/2004 sono:
-
fattore tubo-peritoneale: patologia tubarica acquisita o congenita
-
infertilità maschile di grado moderato
-
endometriosi di III o IV grado
-
endometriosi se la chirurgia o la IUI non hanno dato risultati
-
infertilità inspiegata se il trattamento precedente non ha dato risultati
-
seme crioconservato in relazione alla qualità seminale successiva allo scongelamento
-
fallimento dell’iter terapeutico a bassa tecnologia
La ICSI consiste nell’iniettare all’interno dell’ovocita un singolo spermatozoo.
La ICSI, conosciuta anche come Iniezione intracitoplasmatica degli spermatozoi, consiste nell’iniettare direttamente all’interno dell’ovocita, mediante un particolare microscopio, chiamato micromanipolatore, un singolo spermatozoo.
Gli ovociti vengono denudati dalle cellule del cumulo ooforo che lo circondano e solo quelli maturi (metafase II MII) vengono utilizzati, mentre quelli immaturi (metafase I MI o vescicola germinale VG) vengono valutati come non idonei e scartati.
Dal liquido seminale accuratamente preparato, il biologo seleziona, in base a delle specifiche caratteristiche morfologiche, gli spermatozoi migliori per poi iniettarli all’interno degli ovociti maturi.
Le indicazioni secondo le linee guida della legge 40/2004 sono:
-
infertilità maschile di grado severo
-
azoospermia ostruttiva e secretiva
-
mancata o ridotta fertilizzazione in precedenti cicli FIVET
-
ovociti scongelati
-
ridotto numero di ovociti
-
seme crioconservato in relazione alla qualità seminale successiva allo scongelamento
La ICSI è la tecnica di fecondazione assistita più utilizzata nei centri di fecondazione in vitro, in quanto garantisce alte percentuali di fertilizzazione. Il nostro centro dispone di micromanipolatori ed incubatori di ultima generazione: una garanzia ulteriore dei nostri sforzi, rivolta a dare le massime garanzie possibili alle coppie che si avvalgono dei nostri servizi.
Sono particolari metodiche utilizzate nei casi di assenza di spermatozoi nel liquido seminale.
Nei casi di assenza di spermatozoi nel liquido seminale la causa può un impedimento alla loro emissione (azoospermia ostruttiva) o un’alterazione della spermatogenesi (azoospermia non-ostruttiva).
E’ possibile andare a ricercare l’eventuale presenza degli spermatozoi mediante diverse metodiche:
-
FNA (ago aspirato testicolare): utile nei casi di azoospermia ostruttiva. Con un ago si prelevano direttamente gli spermatozoi presenti del fluido testicolare. Gli spermatozoi così ottenuti possono essere congelati e/o utilizzati per la ICSI
-
Biopsia testicolare
-
TESE (estrazione testicolare degli spermatozoi): Queste procedura consiste nel prelevare chirurgicamente piccole quantità di tessuto testicolare. Può essere effettuata sia in anestesia locale sia in generale. Il tessuto prelevato viene sminuzzato e osservato al microscopio ad alto ingrandimento al fine di determinare la presenza di spermatozoi e/o di spermatidi. Nel caso in cui vengano ritrovati si può procedere al congelamento del tessuto testicolare per poi utilizzarli in ICSI successive.
-
Micro-TESE (estrazione microchirurgica testicolare degli spermatozoi): tecnica chirurgica che utilizza un particolare microscopio sul campo operatorio attraverso il quale vengono analizzati i singoli tubuli seminiferi. Vengono prelevati quelli che appaiono di maggior diametro, più scuri e più vicini ai vasi sanguigni in quanto maggiore è la probabilità che in essi vi siano spermatozoi.
La crioconservazione è il processo che consente di preservare a temperature basse spermatozoi, embrioni e ovociti.
La crioconservazione (comunemente denominata congelamento) è un processo attraverso il quale è possibile preservare a basse temperature e per lunghi periodi di tempo le strutture cellulari e, quindi, anche gli spermatozoi e gli ovociti ed embrioni ottenuti con le tecniche di fecondazione assistita.
Il congelamento di embrioni ed ovociti, rappresenta uno strumento in grado di aumentare le gravidanze ottenute. Con un solo ciclo di induzione dell’iperstimolazione ovarica controllata, infatti, si possono ottenere ovociti o embrioni da utilizzare, in parte subito e/o in parte in cicli successivi, in caso di insuccesso e/o per una eventuale seconda gravidanza.
LA PMA DI TIPO ETEROLOGO
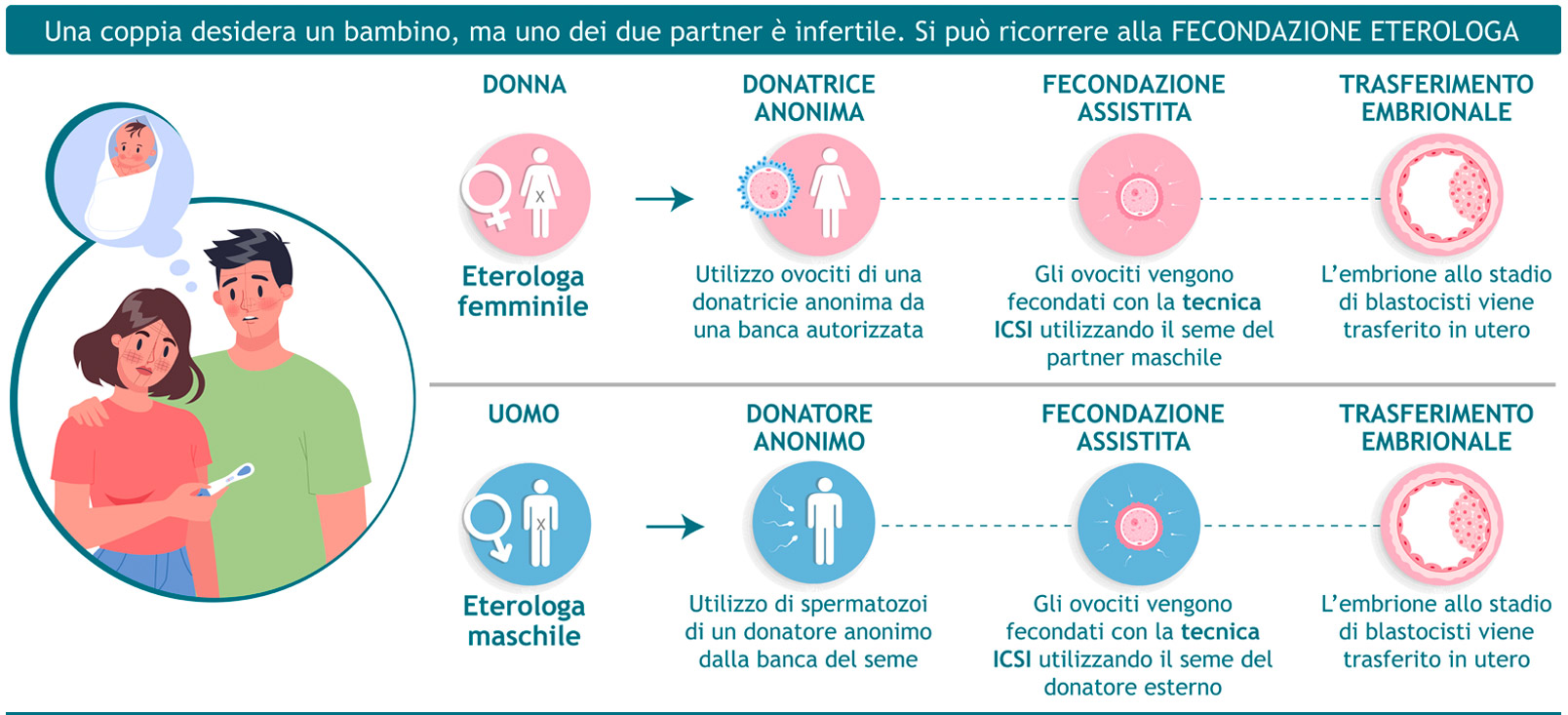
La fecondazione eterologa è una tecnica di PMA che si esegue attraverso la donazione di gameti femminili (ovociti) o maschili (spermatozoi). La donazione dev’essere volontaria, cioè frutto di una scelta intenzionale e consapevole, e disinteressata, ossia non può essere effettuata dietro compenso.
La fecondazione eterologa femminile (OD) prevede l’impiego di spermatozoi appartenenti al partner e di ovociti appartenenti a una donatrice esterna.
La fecondazione eterologa maschile prevede l’impiego di ovociti della partner e di spermatozoi donati (SD).
Mediante la fecondazione eterologa è anche possibile ottenere un embrione con entrambi i gameti donati.
LA FECONDAZIONE ETEROLOGA IN ITALIA
Fino a qualche anno fa, in Italia, vigeva il divieto assoluto di ricorrere a tecniche di PMA di tipo eterologo. Con la sentenza n. 162 del 2014 la Corte costituzionale ha dichiarato illegittimo tale impedimento, ritenendolo lesivo del diritto alla salute e all’autodeterminazione delle coppie. Grazie a questo provvedimento oggi, anche nel nostro Paese, le coppie con diagnosi di sterilità o infertilità possono ricorrere alla donazione per ricercare la gravidanza, purché entrambi i partner siano maggiorenni, di sesso diverso, sposati o conviventi. Resta, a tutt’oggi, in vigore il divieto di ricorrere alla fecondazione eterologa per le donne single e le coppie dello stesso sesso.
LA FECONDAZIONE ETEROLOGA NEL CENTRO PMA DI VILLA MARGHERITA
Dal momento che in Italia, attualmente, esistono pochissimi donatori di cellule riproduttive, i gameti impiegati per le tecniche di PMA di tipo eterologo provengono principalmente da banche di altri paesi europei. Per poter garantire alle coppie la massima affidabilità e una più elevata percentuale di successo nella ricerca della gravidanza, il Centro PMA Villa Margherita ha instaurato una collaborazione tecnico scientifica con una struttura spagnola leader del settore. La struttura prevede una serie di garanzie a tutela della coppia, del nascituro e del donatore.
Selezione e screening dei donatori
I donatori sono selezionati previo accertamento di specifici requisiti soggettivi e caratteristiche fenotipiche, garantendo nei limiti del possibile la compatibilità delle principali caratteristiche fenotipiche del donatore con quelle della coppia ricevente (colore della pelle, occhi e capelli, gruppo sanguigno), nel rispetto dei criteri e delle condizioni di qualità e sicurezza così come previsto dalle Direttive Europee.
Tutti i donatori sono sottoposti agli esami infettivi e genetici a massima tutela dei riceventi, ai sensi del D.lgs. 191/07 e della Dir. 17/2006 all 3, con le modalità e alle condizioni previste dai protocolli medici adottati descritti nelle Direttive Europee.
Potranno essere anche effettuati esami genetici non previsti dagli obblighi di legge, che serviranno ad escludere la possibilità di trasmissione di malattie genetiche.
Numero massimo di donazioni
I gameti (ovociti o spermatozoi) di un unico donatore non potranno determinare più di 10 nascite. Si può prescindere da limite solo nei casi in cui una coppia, che abbia già avuto un figlio, intenda averne un altro dal medesimo donatore (Conferenza Stato regioni 4 settembre 2014 n. 162).
Tutela della privacy, anonimato e relazione parentale
Nel rispetto dell’anonimato e delle disposizioni della privacy vengono resi anonimi tutti i dati, comprese le informazioni genetiche, affinché né il donatore né il ricevente siano identificabili (Decreto legislativo n. 191/2007).
Il contributo della donatrice/donatore è unicamente di tipo genetico. Da un punto di vista legale il genitore legale è colui che ha espresso la volontà di ricorrere alla tecnica di PMA. Il donatore di gameti non acquisisce alcuna relazione giuridica parentale con il bambino, non può essere titolare di obblighi e non può far valere nei suoi confronti alcun diritto (D.lgs n.191/2007).
La PGT consente di identificare negli embrioni specifiche anomalie cromoscomiche numeriche (PGT-A), strutturali (PGT-SR), e di riconoscere embrioni di coppie a rischio di trasmissione di malattie monogeniche (PGT-M).
Con le tecnica di PGT-A possono essere analizzati gameti ed embrioni di coppie con diagnosi di infertilità che fanno richiesta al Responsabile del Centro di PMA di essere informati sullo stato di salute dei loro embrioni (legge 40/2004 art.14 comma 5).
La PGT-A (Test Genetici Preimpianto per Aneuploidie) è una metodologia di diagnosi genetica preimpianto che permette di effettuare lo screening dell’assetto cromosomico di ciascun embrione al fine di identificare eventuali anomalie di tipo numerico (aneuploidie). Con le nuove procedure molecolari di diagnosi è possibile identificare le aneuploidie a carico dei 22 autosomi (cromosomi dal nr. 1 al nr. 22) e dei cromosomi sessuali (X e Y), o anche variazioni del contenuto di piccole porzioni cromosomiche, come amplificazioni (duplicazioni), delezioni e traslocazioni sbilanciate.
Le Indicazioni dell’ESHRE (European Society of Human Reproduction and Embryology) per la PGT-A sono:
- Coppie con Età materna avanzata: la formazione di embrioni con aneuploide è spessa associata all’età materna. La PGT-A è, quindi, consigliata quando l’età della donna è superiore o uguale a 38 anni
- Ripetuti fallimenti d’impianto: nelle coppie che presentano ripetuti fallimenti nei trattamenti di fecondazione assistita anche trasferendo embrioni con buone caratteristiche morfologiche.
- Aborti ripetuti: quando la paziente è andata incontro a due o più aborti non dovuti a problemi meccanici come miomi, malformazioni dell’utero o problemi di coagulazione.
- Mosaicismo cromosomico: nel caso di pazienti che presentano alcune cellule (linee cellulari) con un cariotipo alterato per quanto riguarda i cromosomi sessuali
- Infertilità maschile grave: nel caso di pazienti che devono far ricorso ad una biopsia testicolare per reclutare spermatozoi da utilizzare nelle tecniche di fecondazione assistita.
La PGT-A si effettuata in quinta/sesta o settima giornata sugli embrioni allo stadio di blastocisti e presenta diversi vantaggi:
- Vengono prelevate più cellule (10-20) rispetto all’embrione in terza giornata che presenta 6-8 cellule .Questo comporta una diagnosi più precisa (errore inferiore all’1%) e si riduce sensibilmente il rischio di “mancata diagnosi”.
- La biopsia viene effettuata solo sugli embrioni che sono in grado di arrivare allo stadio di blastocisti.
- Non viene danneggiata la massa cellulare interna che darà vita al feto in quanto le cellule vengono prelevate dal trofoblasto che formerà gli annessi embrionali.
- Gli embrioni che arrivano allo stadio di blastocisti presentano statisticamente un minor tasso di alterazioni cromosomiche.
- Si evita il transfer di embrioni che potrebbero presentare mosaicismo.
PGT-M/PGT sr Diagnosi preimpianto di malattie monogeniche o patologie cromosomiche (numeriche o strutturali)
Con PGT-M/PGT sr si intende l’Identificazione di specifiche anomalie genetiche negli embrioni di coppie a rischio di trasmissione di malattie monogeniche o patologie cromosomiche (numeriche o strutturali).
La legge n°40/2004 dà il diritto ad ogni coppia di sapere lo stato di salute dei propri embrioni (art.14 comma 5) prima che essi siano trasferiti in utero: è quindi possibile eseguire la diagnosi genetica preimpianto in quelle coppie infertili che si apprestano alla procreazione medicalmente assistita (PMA).
Chi dovrebbe avvalersi del test PGT-M?
Le coppie ad alto rischio personale o familiare di mutazioni monogenetiche.
Un’équipe di specialisti uniti per raggiungere il tuo obiettivo.
L’Equipe del Centro PMA di Villa Margherita è a fianco di tutte le coppie, pronto a sostenerle, a prendersi cura di loro e ad accompagnarle nelle principali tappe del nuovo percorso di vita con grande competenza, serietà e umanità.
Ne fanno parte i migliori esperti del settore – ginecologi, andrologi, anestesisti, genetisti, psicologi, biologi, ostetriche, infermieri – uniti da un unico importante obiettivo: aiutare i propri pazienti a realizzare il loro più grande sogno.
Guarda il video del laboratorio di Embriologia.


Un’équipe di specialisti uniti per raggiungere il tuo obiettivo.
L’Equipe del Centro PMA di Villa Margherita è a fianco di tutte le coppie, pronto a sostenerle, a prendersi cura di loro e ad accompagnarle nelle principali tappe del nuovo percorso di vita con grande competenza, serietà e umanità.
Ne fanno parte i migliori esperti del settore – ginecologi, andrologi, anestesisti, genetisti, psicologi, biologi, ostetriche, infermieri – uniti da un unico importante obiettivo: aiutare i propri pazienti a realizzare il loro più grande sogno.
Guarda il video del laboratorio di Embriologia.
I punti di forza del nostro Centro PMA.
Oltre 30 anni
di esperienza
percorsi accanto ad ogni coppia, offrendo un’assistenza completa
e multidisciplinare
Equipe medica
di alto livello
di cui fanno parte medici, biologi
e specialisti di grande esperienza
e professionalità
Tecnologie
all’avanguardia
nel campo della diagnosi, della
cura e del trattamento dei
problemi dell’infertilità
Clinica che ti
segue in tutto
dalla procreazione assistita alla
maternità, dall’ostetricia alla
pediatria
Percorsi PMA
personalizzati
definiti in base alle esigenze
di ogni coppia e al loro quadro
clinico
Metodologie
certificate
rigorosamente eseguite e monitorate
durante ogni
fase del trattamento
Iniziamo a conoscerci.
Fissa un appuntamento.
Il primo incontro è un passo molto importante nel percorso di ogni coppia che desidera avere un bambino. La nostra Equipe avrà cura di gestirlo nella più totale riservatezza, dedicandoti una consulenza mirata e fornendoti, se necessario, tutto il supporto psicologico di cui hai bisogno.
Vuoi prenotare una visita o avere maggiori informazioni?
oppure contattaci al numero:
06 8627 5690
Iniziamo a conoscerci.
Fissa un appuntamento.
Il primo incontro è un passo molto importante nel percorso di ogni coppia che desidera avere un bambino. La nostra Equipe avrà cura di gestirlo nella più totale riservatezza, dedicandoti una consulenza mirata e fornendoti, se necessario, tutto il supporto psicologico di cui hai bisogno.
Vuoi prenotare una visita o avere maggiori informazioni?
oppure contattaci al numero:
06 8627 5690
Hai ancora qualche dubbio? Siamo qui per chiarirtelo.
Il 35% delle cause di sterilità sono di origine femminile, il 35% di origine maschile mentre il 20% è di origine mista attribuibile ad entrambi i partner. Il restante 10% delle cause di sterilità è idiopatica cioè senza causa specifica identificata.
La probabilità di ottenere una gravidanza, a prescindere dalle cause di sterilità, é in funzione dell’età materna. Quando l’età della donna è inferiore ai 35 anni, è probabile che entro il primo anno di rapporti non protetti si instauri una gravidanza. Quando l’età della donna supera i 35 anni il tempo scende ai 6 mesi limite oltre il quale è consigliato rivolgersi ad un centro di fecondazione assistita.
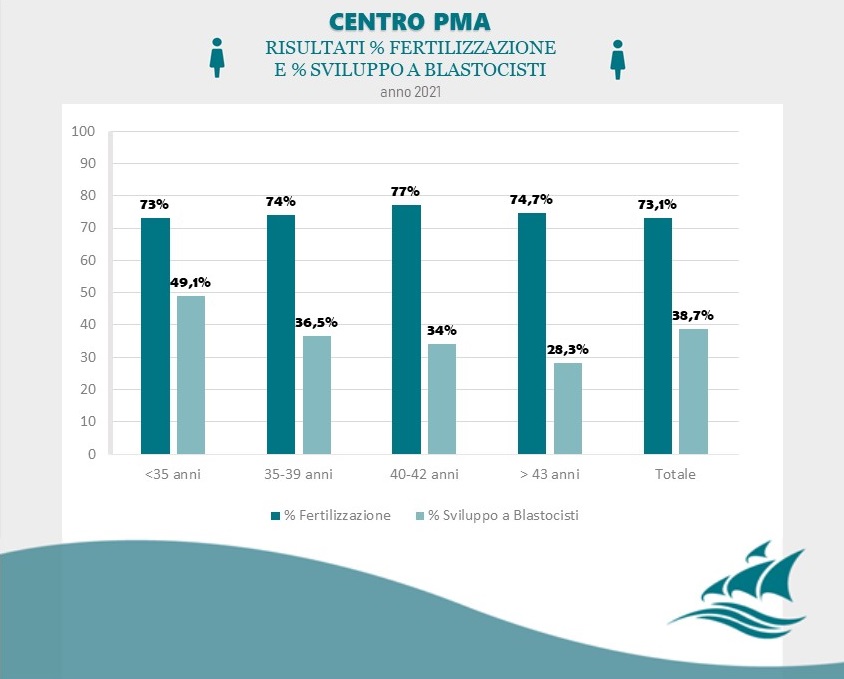
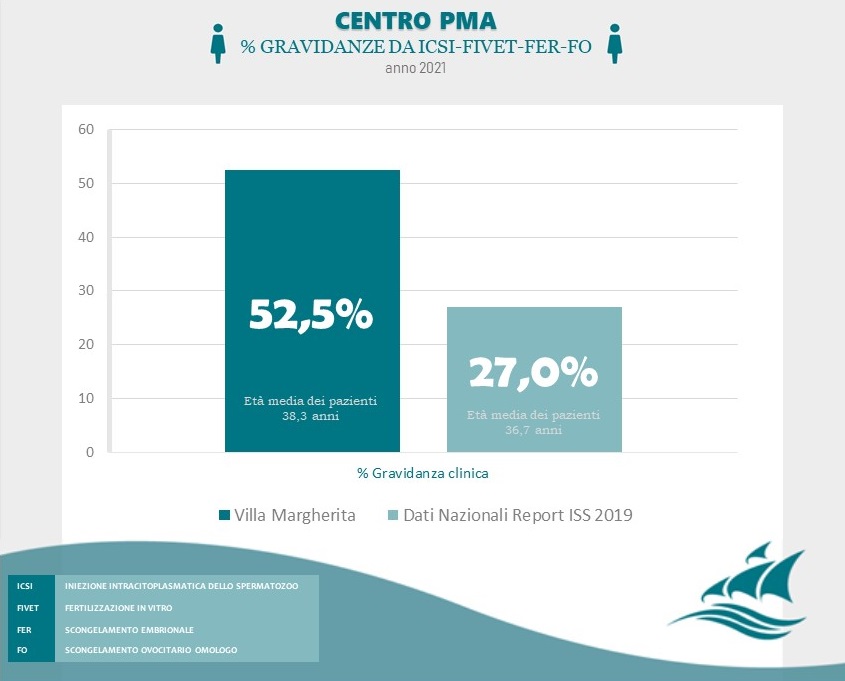
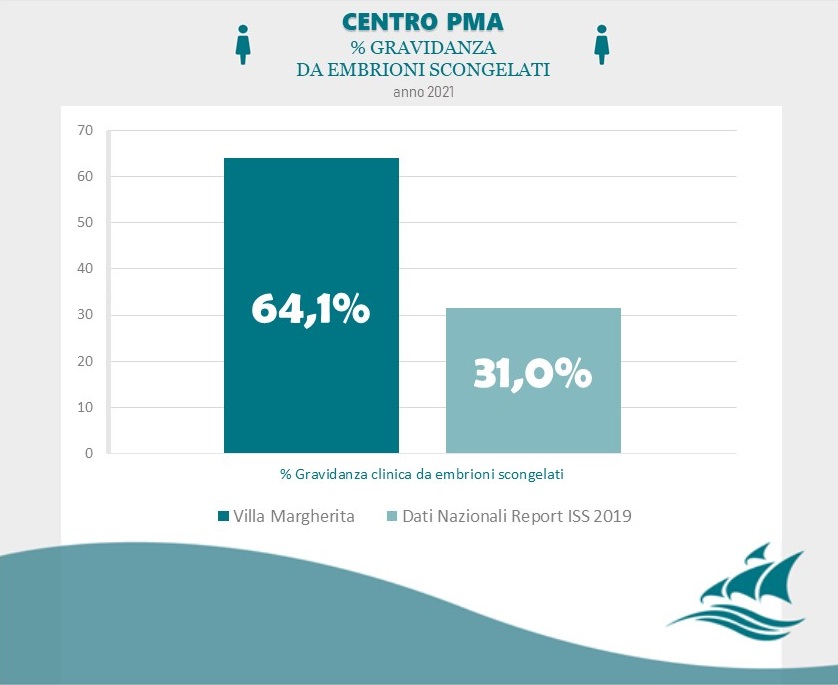
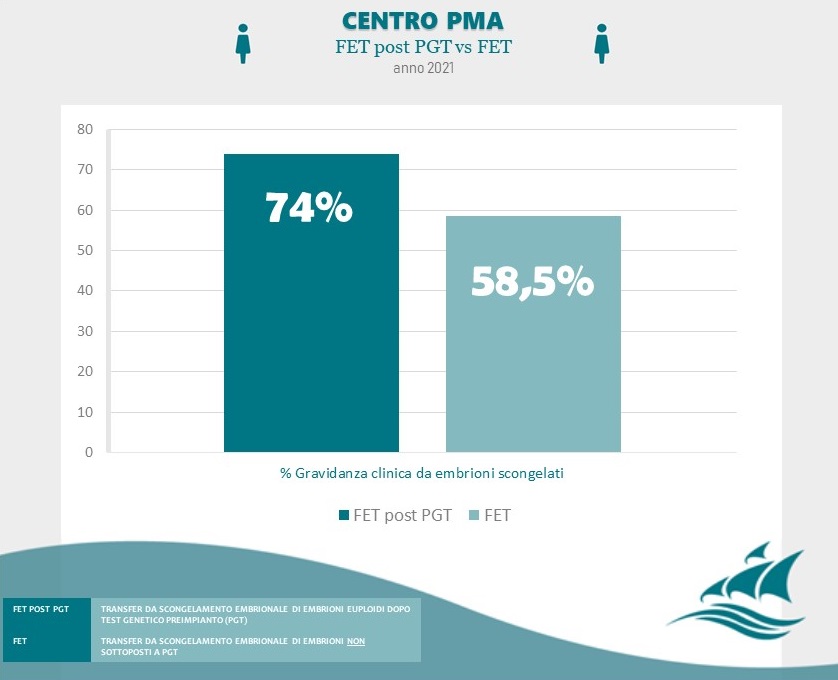
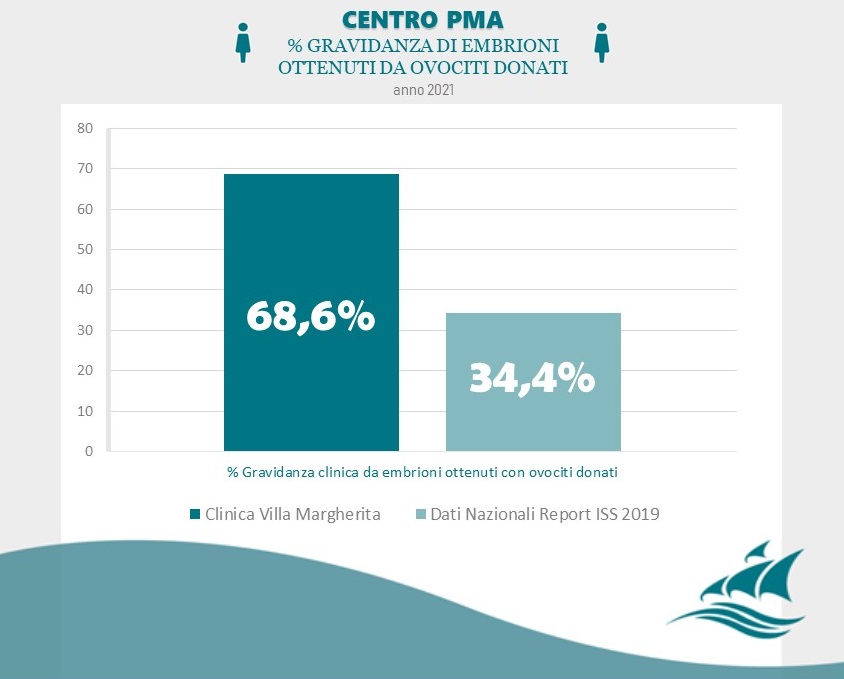
Il principale fattore che influenza le percentuali di successo delle tecniche di fecondazione assistita è l’età materna.
Scopri i nostri risultati cliccando sul seguente link.
Benchè alcuni tumori sia estrogeni dipendenti, non vi è in letteratura nessuna evidenza che indichi una relazione tra tumore alla mammella ed il “bombardamento ormonale” a cui le pazienti pensano di essere sottoposte durante un ciclo di fecondazione assistita. È tuttavia consigliabile, prima di eseguire un trattamento, valutare con il ginecologo di riferimento l’anamnesi familiare per questo tipo di patologie e, nel caso, eseguire una mammografia.
Attualmente grazie alla Consulta (sentenza 151/2009) è possibile a discrezione del ginecologo, in base all’età della paziente ed alle cause di sterilità, fertilizzare anche più di 3 ovociti. Gli eventuali embrioni sopranumerari evolutivi vengono congelati.
Dopo il transfer degli embrioni, per circa 3-4 giorni, è consigliato un periodo di riposo a casa. Successivamente è possibile tornare al lavoro, evitando di stancarsi eccessivamente e di sollevare pesi.
Non è possibile sapere se si è instaurata una gravidanza prima di 12 giorni dal transfer degli embrioni effettuando l’esame della BHCG sul sangue. In caso di positività il prelievo deve essere ripetuto ogni 4 giorni. Sarà possibile evidenziare la camera gestazionale solo dopo 10 giorni dalla prima Beta.
PER ACCEDERE AL PERCORSO PMA, SCARICA I SEGUENTI DOCUMENTI.

Ti accompagnamo, passo dopo passo, verso il risultato
L’Equipe del Centro PMA di Villa Margherita è accanto a tutte le coppie, assistendole durante il loro percorso diagnostico-terapeutico e anche dopo l’ottenimento della gravidanza, fino alla nascita del bambino.
All’interno della struttura polispecialistica Villa Margherita troverai infatti le migliori eccellenze specialistiche nel campo della Ginecologia, Ostetricia, Diagnosi Prenatale e Pediatria in grado di tutelare la salute delle future mamme e dei loro bambini, offrendo prestazioni mediche e diagnostiche di alto livello (visite specialistiche, ecografie ginecologiche e ostetriche, tri test, amniocentesi, villocentesi, corsi pre-parto, screening neonatali, ecc…).

Ti accompagnamo, passo dopo passo, verso il risultato
L’Equipe del Centro PMA di Villa Margherita è accanto a tutte le coppie, assistendole durante il loro percorso diagnostico-terapeutico e anche dopo l’ottenimento della gravidanza, fino alla nascita del bambino.
All’interno della struttura polispecialistica Villa Margherita troverai infatti le migliori eccellenze specialistiche nel campo della Ginecologia, Ostetricia, Diagnosi Prenatale e Pediatria in grado di tutelare la salute delle future mamme e dei loro bambini, offrendo prestazioni mediche e diagnostiche di alto livello (visite specialistiche, ecografie ginecologiche e ostetriche, tri test, amniocentesi, villocentesi, corsi pre-parto, screening neonatali, ecc…).
Consulenza nutrizionale
Le evidenze che correlano la fertilità con la nutrizione sono in continuo aumento. È ormai scientificamente riconosciuto che il sovrappeso e l’obesità costituiscono un importante ostacolo alla fertilità, sia maschile che femminile. È stato dimostrato che una perdita pari al 10% del peso corporeo, anche senza arrivare al peso ideale, può comportare un aumento delle percentuali di gravidanza, sia naturale sia attraverso percorsi di procreazione medicalmente assistita..


Consulenza nutrizionale
In Italia il 12% dei casi di infertilità dipende da eccessivo peso ponderale (17,5%) o da eccessiva magrezza (12%) nella donna.
Lo riferisce uno studio dell’Osservatorio Grana Padano che ha preso in esame circa 5.000 adulti, tra i 20 e i 40 anni. Secondo questa ricerca i casi di infertilità, sia per la donna sia per l’uomo, oltre a essere in aumento, sono causati perlopiù da patologie specifiche che possono ostacolare il concepimento, quali per esempio il varicocele e l’endometriosi, ma talvolta sono attribuibili a uno stile di vita non corretto e al concorso di fattori ambientali come il fumo, lo stress e l’alimentazione sbilanciata.

Consulenza genetica
La consulenza genetica è un passaggio imprescindibile del percorso che porta all’esecuzione di un test genetico.
In sede di consulenza si stabiliscono, sulla base dell’anamnesi familiare, personale e di quelle che possono essere le possibilità diagnostiche disponibili, gli eventuali test genetici eseguibili. La consulenza genetica è un momento indispensabile per la corretta comprensione dei limiti e dell’attendibilità di un test genetico.
Il colloquio con un genetista risulta utile anche nella programmazione di una gravidanza e nella scelta del miglior iter diagnostico da seguire a gravidanza avviata.

Consulenza genetica
La consulenza genetica è un passaggio imprescindibile del percorso che porta all’esecuzione di un test genetico.
In sede di consulenza si stabiliscono, sulla base dell’anamnesi familiare, personale e di quelle che possono essere le possibilità diagnostiche disponibili, gli eventuali test genetici eseguibili. La consulenza genetica è un momento indispensabile per la corretta comprensione dei limiti e dell’attendibilità di un test genetico.
Il colloquio con un genetista risulta utile anche nella programmazione di una gravidanza e nella scelta del miglior iter diagnostico da seguire a gravidanza avviata.
Supporto psicologico
Il percorso per giungere alla richiesta della fecondazione assistita può avere, diversamente per ognuno, importanti ripercussioni psicologiche ed emotive, sia personali che nelle dinamiche di coppia. Molto dipende dalla storia vissuta prima di arrivare a scegliere la PMA, da quanto tempo si cerca di diventare genitori senza riuscirci, dall’esperienza di eventuali interruzioni di gravidanza, dalle pressioni sociali che potrebbero aver circondato la coppia, dal loro carico emotivo e dal tipo di diagnosi ricevuta. Proprio in considerazione delle importanti implicazioni psicologiche legate all’infertilità e ai trattamenti di procreazione assistita, la legge 40/2004 prevede che i centri che se ne occupano mettano a disposizione dei pazienti un servizio di consulenza psicologica.


Supporto psicologico
Il percorso per giungere alla richiesta della fecondazione assistita può avere, diversamente per ognuno, importanti ripercussioni psicologiche ed emotive, sia personali che nelle dinamiche di coppia. Molto dipende dalla storia vissuta prima di arrivare a scegliere la PMA, da quanto tempo si cerca di diventare genitori senza riuscirci, dall’esperienza di eventuali interruzioni di gravidanza, dalle pressioni sociali che potrebbero aver circondato la coppia, dal loro carico emotivo e dal tipo di diagnosi ricevuta. Proprio in considerazione delle importanti implicazioni psicologiche legate all’infertilità e ai trattamenti di procreazione assistita, la legge 40/2004 prevede che i centri che se ne occupano mettano a disposizione dei pazienti un servizio di consulenza psicologica.
Fissa ora un appuntamento.
Il primo incontro è un passo molto importante nel percorso di ogni coppia che desidera avere un bambino. La nostra Equipe avrà cura di gestirlo nella più totale riservatezza, dedicandoti una consulenza mirata e fornendoti, se necessario, tutto il supporto psicologico di cui hai bisogno.
Vuoi prenotare una visita o avere maggiori informazioni?
Compila il form oppure contattaci al numero:
06 8627 5690
Fissa ora un appuntamento.
Il primo incontro è un passo molto importante nel percorso di ogni coppia che desidera avere un bambino. La nostra Equipe avrà cura di gestirlo nella più totale riservatezza, dedicandoti una consulenza mirata e fornendoti, se necessario, tutto il supporto psicologico di cui hai bisogno.
Vuoi prenotare una visita o avere maggiori informazioni?
Compila il form
oppure contattaci ai numeri:
06 86275690 | 06 86275830
Il Dottor Francesco Bartolozzi in qualità di Direttore Sanitario della Clinica Privata Villa Margherita, di proprietà di Villa Margherita Spa, dichiara sotto la propria responsabilità che il messaggio informativo contenuto in questo sito è diramato nel rispetto delle linee guida contenute nelle 'Direttive per l'autorizzazione della pubblicità e dell'informazione sui siti internet e per l'uso della posta elettronica per motivi clinici - Delibera n. 129 del 2007 del Consiglio Direttivo dell'Ordine dei Medici di Roma'.